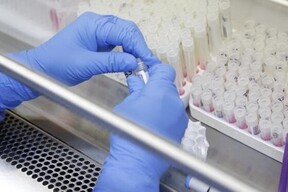
Instituto Nacional de Salud autorizó un total de 60 ensayos clínicos en el Perú durante el 2024
Nota de prensaCifra representa un incremento del 40% en comparación con el año anterior


23 de enero de 2025 - 1:36 p. m.
En el marco de las competencias que desarrolla en el ámbito de la ciencia, el Instituto Nacional de Salud (INS) es la autoridad que autoriza los ensayos clínicos en el Perú. Además, se encarga de velar por el cumplimiento de las normas que regulan estos ensayos a través de la Dirección de Investigación e Innovación en Salud (DIIS).
Como entidad regulatoria, el INS tiene como objetivo es velar por la protección a los sujetos de investigación que participan de un ensayo clínico, garantizando el respeto a sus derechos, autonomía y bienestar. Los ensayos clínicos son autorizados y fiscalizados en conformidad con la regulación nacional, estándares y directrices internacionales de buenas prácticas clínicas.
Es asi que, al cierre del 2024, el INS autorizó un total de 60 ensayos clínicos, lo que representa un 40% más de la cifra obtenida en el 2023, donde se autorizaron 37 ensayos clínicos.
Es asi que, al cierre del 2024, el INS autorizó un total de 60 ensayos clínicos, lo que representa un 40% más de la cifra obtenida en el 2023, donde se autorizaron 37 ensayos clínicos.
Cabe indicar que, de los ensayos clínicos autorizados, casi la tercera parte están dirigidos a beneficiar a personas con enfermedades oncológicas. Asimismo, el tiempo promedio de evaluación de las solicitudes de autorización de ensayos clínicos se redujo en un 36%.
Además, en su rol de fiscalización y con el objetivo de garantizar la realización de ensayos clínicos dentro de las Buenas Prácticas Clínicas, el INS realizó 23 inspecciones en los diferentes Centros de Investigación que tienen ensayos clínicos activos en Lima y otras regiones del país.
Es importante tener en cuenta que, para solicitar la autorización de un ensayo clínico, se debe:
Es importante tener en cuenta que, para solicitar la autorización de un ensayo clínico, se debe:
- Registrarse en el Registro Peruano de Ensayos Clínicos (REPEC)
- Completar el formulario FOR-OGITT-028 Ed3
- Imprimir y firmar el formulario
- Presentar los documentos requeridos
- Pagar el costo de la solicitud
El INS autoriza los ensayos clínicos que cumplen con la regulación vigente y es una base de datos pública que publica información sobre los ensayos clínicos autorizados en el Perú. La autorización se emite mediante una Resolución Directoral.
Cabe destacar que el desarrollo de ensayos clínicos, ofrece a los países la oportunidad de validar nuevas tecnologías al promover alternativas de nuevos tratamientos, estimular el desarrollo económico y contribuir a las iniciativas de salud globales con la mayor generación de investigación. Más información sobre registro de ensayos clínicos en https://ensayosclinicos-repec.ins.gob.pe/